Biosimilars สำคัญอย่างไร
Biosimilars ชื่อนี้หลายคนอาจยังคงสงสัยว่ายากลุ่มนี้มีความสำคัญอย่างไร คำว่า biosimilars หรือชีววัตถุคล้ายคลึงนั้น ตามประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง เอกสารหลักฐานการขอขึ้นทะเบียนตำรับยาชีววัตถุคล้ายคลึง ปี พ.ศ. 2556 หมายถึง “ยาชีววัตถุที่มีลักษณะคล้ายคลึงกันในแง่คุณภาพ ความปลอดภัย และประสิทธิภาพ เมื่อเปรียบเทียบกับยาชีววัตถุอ้างอิงที่ได้รับการขึ้นทะเบียนแล้วอย่างเต็มรูปแบบ” ซึ่งที่จริงแล้วยากลุ่มนี้เป็นยาที่ผลิตขึ้นมาโดยเทคโนโลยีที่คัดลอกโมเลกุลมาจากยาชีววัตถุที่ผ่านการขึ้นทะเบียนและครบระยะเวลาของสิทธิบัตรยาแล้ว โดยตามหลักการแล้วควรจะมีคุณลักษณะเหมือนยาต้นแบบ
ยาชีววัตถุ และยาชีววัตถุคล้ายคลึง คืออะไร
ยาชีววัตถุ หมายถึง ผลิตภัณฑ์ที่มีตัวยาสำคัญที่ผลิตหรือได้มาจากสิ่งมีชีวิต (living organism) เช่น ยาอินซูลินที่ผลิตขึ้นจากสิ่งมีชีวิต (แบคทีเรียหรือยีสต์) ที่มีการตัดต่อใส่ยีนที่ผลิตอินซูลินออกมา หรือวัคซีน หรือผลิตภัณฑ์เลือด หรือที่ได้มาจากพลาสมา เนื่องจากคำว่า “ยา” ตามพระราชบัญญัติยา พ.ศ. 2510 มีความหมายว่าเป็นตัวยาสำคัญหรือผลิตภัณฑ์สำเร็จรูปก็ได้ ดังนั้น ผลิตภัณฑ์ยาชีววัตถุจึงอาจเรียกให้สั้นลงว่ายาชีววัตถุก็ได้
คำว่า “ผลิตภัณฑ์ยาชีววัตถุคล้ายคลึง” หรือเรียกตามคำศัพท์ภาษาอังกฤษแบบเต็มว่า similar biological medicinal products หมายถึง ยาชีววัตถุที่มีความคล้ายคลึง (similar) กับยาชีววัตถุที่ได้รับการอนุญาต ขึ้นทะเบียนและวางจำหน่ายในตลาดมาก่อนแล้ว (มักจะเรียกว่ายาชีววัตถุอ้างอิงซึ่งมักเป็นยาชีววัตถุต้นแบบ) คำศัพท์ภาษาอังกฤษที่นิยมและยอมรับมากที่สุดคือ biosimilars หรือ similar biotherapeutic products (SBP) (ตามการใช้ขององค์การอนามัยโลก) ในปัจจุบันยาชีววัตถุคล้ายคลึงนำมาใช้เรียกเฉพาะกับผลิตภัณฑ์ชีววัตถุประเภทโปรตีนที่ได้มาจากกระบวนการเทคโนโลยีชีวภาพเท่านั้น เพราะเป็นผลิตภัณฑ์ที่สามารถทำให้บริสุทธิ์ได้สูง (highly purified) และ ตรวจสอบลักษณะได้เป็นอย่างดี (well-characterized) ซึ่งตามหลักการแล้วประโยชน์ที่ได้จากการผลิตยากลุ่มนี้จะทำให้ลดต้นทุนได้มาก และมีข้อมูลของยาที่เป็นยาชีววัตถุต้นแบบ
ยาชีววัตถุ (biological products) เป็นยาที่ผลิตขึ้นโดยใช้เทคนิคทางเทคโนโลยีชีวภาพในการผลิต เช่น พันธุวิศวกรรม (genetic engineering) หรือรีคอมบิแนนต์ดีเอ็นเอเทคโนโลยี (recombinant DNA technology) เป็นต้น ยาในกลุ่มนี้มีบทบาทมากขึ้นในการรักษาโรคในปัจจุบัน เช่น โรคมะเร็ง เบาหวาน ไขข้อรูมาตอยด์ การปลูกถ่ายอวัยวะ เป็นต้น
ในปัจจุบันมูลค่าทางการตลาดของยาชีววัตถุทั่วโลกเพิ่มสูงขึ้น และแนวโน้มในอนาคตคาดว่าอัตราการเติบโตด้านการตลาดของยาชีววัตถุจะมีอัตราการเติบโตประมาณ 2 เท่าของยาที่ได้จากการสังเคราะห์ทางเคมี (ยาเคมี) หรือเรียกว่ายาที่มีโมเลกุลขนาดเล็ก (small molecule drugs) และการเริ่มหมดสิทธิบัตรของยาชีววัตถุรุ่นแรก ๆ เรียกว่ายาชีววัตถุต้นแบบ (originator/innovator products) ซึ่งจะทำให้ในอนาคตอันใกล้จะมียาที่ผลิตเลียนแบบยาชีววัตถุต้นแบบ เรียกว่า ไบโอซิมิลาร์ หรือยาชีววัตถุคล้ายคลึง (biosimilars) ในท้องตลาดจำนวนมาก
ปัญหาของยาชีววัตถุและยาชีววัตถุคล้ายคลึง
ยาชีววัตถุส่วนใหญ่เป็นโปรตีน หรือไกลโคโปรตีน คุณลักษณะเฉพาะคือ โมเลกุลมีขนาดใหญ่กว่ายาเคมี 10-1,000 เท่า โครงสร้างทุกระดับของโปรตีนมีความสำคัญต่อการจับกับเป้าหมายยา (drug target) และส่งผลต่อการออกฤทธิ์ทางชีวภาพ ขั้นตอนต่าง ๆ ของกระบวนการผลิต เช่น การเลือก expression vector ชนิดของเซลล์เจ้าบ้าน (host cells) สภาวะในการเลี้ยงเซลล์ การสกัดและการทำให้บริสุทธิ์ การตั้งสูตรตำรับ ตลอดจนการเก็บรักษาและการขนส่งมีความสำคัญมากต่อคุณภาพและประสิทธิภาพของยา เนื่องจากยาชีววัตถุมีความไวต่อสภาวะแวดล้อมจึงมักมีปัญหาเรื่องความไม่คงสภาพของยาหากมีการเก็บรักษายาที่อุณหภูมิไม่เหมาะสม และเนื่องจากขนาดโมเลกุลที่ใหญ่มาก ยาชีววัตถุจึงอาจกระตุ้นภูมิคุ้มกันของร่างกายได้มากกว่ายาเคมี เช่น การกระตุ้นร่างกายให้สร้างแอนติบอดีที่จำเพาะต่อยาที่ได้รับอาจก่อให้เกิดอาการอันไม่พึงประสงค์ตามมาได้ จากการวิจัยพบว่าการเก็บรักษาและการขนส่งยาชีววัตถุที่ไม่เหมาะสมทำให้โครงสร้างของยาเปลี่ยนไป และอาจเกิดจากความผันแปรในกระบวนการผลิตยาชีววัตถุที่มาจากแหล่งผลิตที่แตกต่างกัน ดังนั้น เมื่อมียาที่ผลิตเลียนแบบยาชีววัตถุต้นแบบเรียกว่า ไบโอซิมิลาร์ (biosimilars) หรือยาชีววัตถุคล้ายคลึง (similar biological medicinal products) ซึ่งไม่เหมือนกับยาสามัญ (generic drugs) ที่เป็นยาเคมี เพราะกระบวนการผลิตยาชีววัตถุมีความยุ่งยากซับซ้อนมากกว่า ดังนั้น ขั้นตอนการผลิตไบโอซิมิลาร์ที่ต่างไปจากการผลิตยาชีววัตถุต้นแบบเพียงเล็กน้อยก็อาจส่งผลต่อคุณภาพยาและความปลอดภัยจากการใช้ยา โดยเฉพาะอย่างยิ่งในเรื่องการกระตุ้นภูมิคุ้มกันของร่างกายซึ่งอาจทำให้เกิดอันตรายต่อผู้ใช้ยาได้ ดังนั้น หลักเกณฑ์ในการขึ้นทะเบียนยาและการพิจารณาไบโอซิมิลาร์จึงต้องพิจารณาอย่างละเอียดรอบคอบเป็นพิเศษ
ลักษณะโมเลกุลของยาชีววัตถุ แบ่งออกเป็น
- แบบที่มีโมเลกุลไม่ซับซ้อนมาก
แบบที่มีโมเลกุลไม่ซับซ้อนมากและง่ายต่อการพิสูจน์หรือแยกสาร ตัวอย่างเช่น อินซูลิน เป็นเปปไทด์ฮอร์โมนที่มีโครงสร้างโมเลกุลไม่ซับซ้อน เปรียบเทียบและลอกแบบได้โดยตรง
- แบบที่มีโมเลกุลที่มีความซับซ้อนมาก
ยาชีววัตถุคล้ายคลึงบางกลุ่ม เช่น interferon, epoetin, monoclonal antibody เป็นต้น เป็นโปรตีนที่มีกลุ่มน้ำตาลเกาะอยู่ในโมเลกุล (glycosylated protein) หรือมี isoform ที่ต่างกัน โมเลกุลลักษณะนี้จึงมีความซับซ้อนมากกว่าและยากที่จะพิสูจน์คุณลักษณะ ดังนั้น ความแตกต่างในกระบวนการผลิตของโมเลกุลประเภทนี้อาจส่งผลต่อคุณสมบัติด้านโครงสร้าง ความแตกต่างทางเภสัชพลศาสตร์และเภสัชจลนศาสตร์ ทำให้เกิดความแตกต่างในด้านความปลอดภัยและประสิทธิภาพ และการเกิดอาการไม่พึงประสงค์จากการใช้ยา
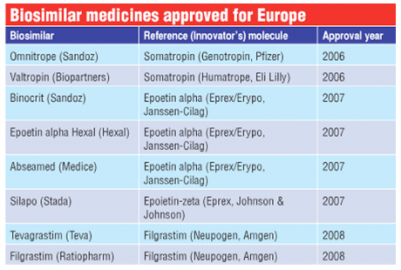
ตารางที่ 1 ตัวอย่างยา biosimilar ที่ขึ้นทะเบียนแล้วในยุโรป(5)
จากบทความข้างต้นที่กล่าวมานั้น ถ้ายาชีววัตถุคล้ายคลึงชนิดนั้นมีคุณสมบัติและประสิทธิภาพได้เท่าเทียมยาต้นแบบจะทำให้โอกาสการเข้าถึงยาของผู้ป่วยนั้นมากขึ้นเพราะต้นทุนที่ถูกลง แต่ถ้าเกิดการเปลี่ยนแปลงระหว่างการผลิตดังที่กล่าวก็อาจเกิดอันตรายได้ ดังนั้น ในการเลือกใช้คงต้องศึกษากันให้ละเอียดในแต่ละตัวยาเพื่อความปลอดภัยของผู้ป่วย
เอกสารอ้างอิง
- อนันต์ชัย อัศวเมฆิน. ยาชีววัตถุคล้ายคลึง (Biosimilars). http://www.pharmacy.mahidol.ac.th/th/knowledge/article/183ยาชีววัตถุคล้ายคลึง-Biosimilars/
- สุชาติ จองประเสริฐ. ยาชีววัตถุคล้ายคลึง (Biosimilars) ในบริบทสาธารณสุข. http://journal.fda.moph.go.th/journal/012557/02.pdf
- ประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง เอกสารหลักฐานการขอขึ้นทะเบียนตํารับยาชีววัตถุคล้ายคลึง. วันที่ 4 ธันวาคม พ.ศ. 2556.
- FDA Approves New Insulin Glargine Basaglar – The First “Biosimilar” Insulin in the US. https://diatribe.org/fda-approves-new-insulin-glargine-basaglar-first-biosimilar-insulin-us
- Biologics with a greater reach. http://www.biospectrumindia.com/biospecindia/news/155949/biologics-reach