ภาวะเลือดออกในเยื่อหุ้มสมอง (Subarachnoid hemorrhage)
อ.นพ.สันติ สิลัยรัตน์ คณะแพทยศาสตร์วชิรพยาบาล มหาวิทยาลัยนวมินทราธิราช
ภาวะเลือดออกในเยื่อหุ้มสมอง (subarachnoid hemorrhage) โดยไม่มีประวัติการได้รับการบาดเจ็บที่บริเวณศีรษะมาก่อน ราวร้อยละ 80 มีสาเหตุมาจากการแตกของหลอดเลือดในสมองที่เกิดการโป่งพอง (intracranial aneurysm) ส่วนสาเหตุอื่น ๆ ที่อาจพบได้มักจะมาจากการสร้างหลอดเลือดผิดปกติ (vascular malformation) หรือจากการอักเสบของหลอดเลือด (vasculitis) มีส่วนน้อย (ประมาณร้อยละ 10) ไม่พบความผิดปกติของหลอดเลือดในสมอง ภาวะนี้มักจะพบในกลุ่มคนอายุน้อยมากกว่าผู้สูงอายุ และมีความสำคัญมากเนื่องจากมักทำให้เกิดความพิการหรือความผิดปกติถาวรได้ถึงประมาณครึ่งหนึ่งของผู้ป่วยทั้งหมด ซึ่งทำให้สูญเสียคุณภาพชีวิตอย่างมาก
โรคหลอดเลือดในสมองโป่งพอง (Intracranial aneurysms)
การโป่งพองของหลอดเลือดในสมองเกิดขึ้นได้ประมาณ 1-2% ของประชากร ตำแหน่งที่เกิดการโป่งพองมักจะเป็นจุดที่หลอดเลือดแดงมีการแยกสาขาออกจากกัน เนื่องจากเป็นบริเวณที่ได้รับแรงเซาะหรือกระทบจากกระแสเลือดอยู่ตลอดเวลา ผู้ที่มีความเสี่ยงต่อการเกิดภาวะนี้ ได้แก่ ผู้ที่มีประวัติภาวะนี้ในครอบครัว (โดยเฉพาะอย่างยิ่งตั้งแต่ 2 คนขึ้นไป) มีโรคที่เกี่ยวข้องกับเนื้อเยื่อเกี่ยวพัน (connective tissue disorders) เช่น Ehlers-Danlos syndrome และในผู้ป่วยโรค polycystic kidney disease ส่วนความเสี่ยงที่จะเกิดการแตกของหลอดเลือดที่โป่งพอง ได้แก่ เชื้อชาติ (กลุ่มคนผิวดำและละติน) การมีความดันโลหิตสูง สูบบุหรี่ ดื่มแอลกอฮอล์ มีการใช้ยาในกลุ่ม sympathomimetic drugs และการมีขนาดของ aneurysm ใหญ่กว่า 7 มิลลิเมตรขึ้นไป
อุบัติการณ์ของการเกิดเลือดออกจากหลอดเลือดสมองโป่งพองนั้นมีความแตกต่างกันไปในแต่ละการศึกษาตั้งแต่ 2.0 รายต่อประชากร 100,000 รายในประเทศจีน ไปจนถึง 22.5 รายต่อประชากร 100,000 รายในประเทศฟินแลนด์ ทั้งนี้อาจเป็นความถี่ของการตรวจค้นในแต่ละพื้นที่ และเนื่องจากในปัจจุบันการตรวจสมองด้วยวิธี computed tomography (CT) และ magnetic resonance imaging (MRI) เพิ่มมากขึ้นจึงทำให้สามารถตรวจพบภาวะนี้ได้บ่อยกว่าแต่ก่อน สำหรับในประเทศสหรัฐอเมริกา ข้อมูลอุบัติการณ์ของโรคในปี ค.ศ. 2003 อยู่ที่ 14.5 รายต่อประชากร 100,000 รายต่อปี ภาวะนี้พบได้บ่อยในกลุ่มผู้หญิงและพบได้มากขึ้นเมื่ออายุมากขึ้น และมากสุดในช่วงวัย 40-50 ปี
เมื่อหลอดเลือดในสมองที่โป่งพองเกิดการแตก เลือดจะออกมาจากหลอดเลือดแดงเข้าสู่ชั้นเยื่อหุ้มสมองส่วน subarachnoid space และเกิดการสะสมแรงดันในบริเวณดังกล่าวเพิ่มขึ้นเรื่อย ๆ จนเท่ากับแรงดันภายในหลอดเลือดแล้ว และมีการสร้างลิ่มเลือดขึ้นแล้วภาวะเลือดออกจึงจะหยุดลง ดังนั้น การมีเลือดออกจากหลอดเลือดเหล่านี้จึงสร้างผลกระทบกับสมองได้มาก และมีผู้ป่วยถึงร้อยละ 25-50 ที่เสียชีวิตจากภาวะนี้
อาการและอาการแสดงของภาวะ Subarachnoid hemorrhage
ลักษณะอาการที่เด่นชัดเมื่อเกิดมีเลือดออกจากหลอดเลือดในสมองคือ อาการปวดศีรษะซึ่งมักจะรุนแรงมากและเกิดขึ้นอย่างทันที อาการปวดมักจะเพิ่มขึ้นจนถึงจุดสูงสุดภายในเวลาไม่กี่วินาที (จึงมักจะถูกเรียกว่า thunderclap headache) ผู้ป่วยราวร้อยละ 10-40 อาจเริ่มมีอาการปวดศีรษะนำมาก่อนคล้ายสัญญาณเตือน (“sentinel” headache) ก่อนเกิดมีเลือดออกจริงประมาณ 2-8 สัปดาห์ ซึ่งมักจะเกิดจากการเริ่มมีเลือดรั่วออกมาจากหลอดเลือด ผู้ป่วยที่มีเลือดออกอาจให้ประวัติการทำกิจกรรมที่หนักหรือมีความเครียดในช่วงที่เกิดอาการก็ได้ แต่โดยมากแล้วสามารถเกิดภาวะเลือดออกได้แม้จะเป็นการทำกิจกรรมในชีีวิตประจำวัน อาการและอาการแสดงอื่น ๆ ที่อาจพบร่วมด้วย ได้แก่ อาการคลื่นไส้ อาเจียน ตาสู้แสงไม่ได้ (photophobia) คอตึงแข็ง (neck stiffness) มีความผิดปกติของระบบประสาทเฉพาะที่ (focal neurologic deficits) และในบางรายอาจมีอาการหมดสติชั่วคราวได้ สำหรับผู้ป่วยที่มีเลือดออกอย่างรุนแรงอาจพบมีระดับความรู้สึกตัวที่ลดลงไปจนถึงโคม่าได้ ซึ่งระดับความผิดปกติของอาการและอาการแสดงเมื่อแรกวินิจฉัยที่มาก บ่งบอกถึงแนวโน้มการพยากรณ์โรคที่ไม่ดี
เนื่องจากอาการปวดศีรษะที่เกิดขึ้นจาก subarachnoid hemorrhage นั้นมักจะพบได้เพียงร้อยละ 1 ของผู้ป่วยทั้งหมดที่มารับการรักษาที่ห้องฉุกเฉินด้วยอาการปวดศีรษะ ดังนั้น ผู้ป่วยภาวะนี้มักจะถูกวินิจฉัยเป็นโรคหรือความผิดปกติอื่นที่พบได้บ่อยกว่า เช่น ไมเกรน (migraine) หรืออาการในกลุ่ม functional headache อื่น ๆ ที่ไม่จำเป็นต้องทำการตรวจวินิจฉัยเพิ่มเติม ทำให้ผู้ป่วยมีโอกาสเกิดความพิการหรือเสียชีวิตได้มากจากการไม่ได้รับการวินิจฉัยที่ถูกต้องทันเวลา ดังนั้น จึงควรนึกถึงและสงสัยภาวะนี้เอาไว้เสมอหากผู้ป่วยมีลักษณะอาการหรืออาการแสดงที่กล่าวมา
แนวทางในการดูแลรักษาภาวะเลือดออกในเยื่อหุ้มสมอง
การตรวจประเมินผู้ป่วย เมื่อผู้ป่วยมาถึงมือแพทย์ เป้าหมายแรกของการรักษาคือ การพยายามลดโอกาสของการเกิดและแก้ไขภาวะแทรกซ้อนที่เกิดขึ้นจากการมีเลือดออก โดยเฉพาะในแง่ของการทำงานของสมองให้ได้มากที่สุด โดยขั้นต้นควรให้ดูแลทางเดินหายใจให้เปิดโล่งและมีระบบไหลเวียนเลือดทำงานที่เป็นปกติ ควบคุมและป้องกันอาการชัก จากนั้นจึงพิจารณาทำการตรวจวินิจฉัยในขั้นตอนต่อไป
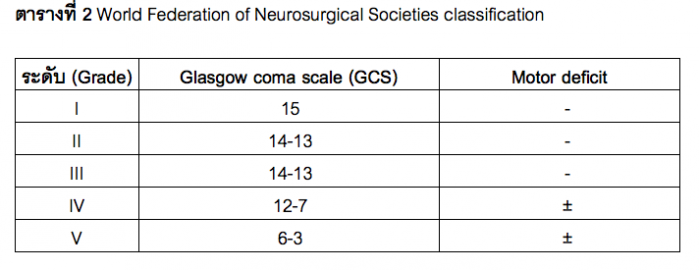
Grading system ที่ใช้ในการประเมินผู้ป่วย ในปัจจุบันมีการเสนอ grading system สำหรับใช้ในการประเมินผู้ป่วย subarachnoid hemorrhage เอาไว้หลายแบบ ซึ่งโดยมากแล้วจะพยายามหาความสัมพันธ์เชื่อมโยงระหว่างอาการและอาการแสดงเมื่อแรกวินิจฉัยกับการพยากรณ์โรคหลังการรักษาเป็นสำคัญ รูปแบบของ grading system ที่นิยมใช้อยู่ในปัจจุบันมี 2 แบบคือ World Federation of Neurosurgical Societies classification และ Hunt-Hess classification ซึ่งทั้ง 2 แบบให้ความสำคัญกับความรุนแรงของการเกิดความผิดปกติที่สมอง (encephalopathy) มากที่สุด ส่วนความผิดปกติอื่นที่นำมาใช้ในการประเมินร่วมกัน ได้แก่ ความผิดปกติของระบบประสาทเฉพาะที่หรืออาการแขนขาอ่อนแรง อาการคอแข็ง (nuchal rigidity) เป็นต้น
ตารางที่ 1 Hunt-Hess classification สำหรับการประเมิน subarachnoid hemorrhage
ตารางที่ 2 World Federation of Neurosurgical Societies classification
การตรวจทางรังสีวิทยา การตรวจขั้นต้นที่จำเป็นในการวินิจฉัย ได้แก่ การตรวจ CT สมองโดยไม่ฉีดสารทึบแสง การตรวจด้วยวิธีนี้มีความไวมากถึง 100% ภายใน 3 วันแรกหลังเกิดโรค แต่จะลดลงเหลือประมาณ 50% หลังจากเกิดโรคไปแล้ว 5-7 วัน บางรายอาจพบมีก้อนเลือด (hematoma) หรือมีน้ำในสมอง (hydrocephalus) ร่วมด้วยได้ ซึ่งเป็นภาวะแทรกซ้อนที่ต้องรีบให้การรักษาโดยการผ่าตัดในทันที สำหรับในรายที่ลักษณะอาการและอาการแสดงเข้าได้ชัดเจนหรือยังมีข้อสงสัยแต่ผลการตรวจ CT ไม่พบความผิดปกติควรทำการตรวจเพิ่มเติมในขั้นต่อไป
การเจาะเก็บน้ำไขสันหลัง (lumbar puncture) เป็นวิธีการหนึ่งที่มีการนำมาใช้เพื่อการวินิจฉัย โดยการตรวจหาเม็ดเลือดหรือลักษณะแบบ xanthochromia ในน้ำหล่อเลี้ยงสมองและไขสันหลัง (cerebrospinal fluid) แต่ในระยะหลังการทำ lumbar puncture เพื่อการวินิจฉัยเลือดออกในกรณีที่การตรวจ CT ไม่พบความผิดปกตินั้นลดลงไปมากเนื่องจากมีการตั้งข้อสังเกตว่าวิธีการนี้ไม่มีประโยชน์ในการช่วยวินิจฉัยชัดเจน และมีข้อมูลว่าการตรวจด้วย MRI ด้วยเทคนิค fluid-attenuation inversion recovery, proton density และ gradient-echo sequences นั้นมีความไวต่อการตรวจหาสาร heme ที่อยู่ใน CSF กว่ามาก
สำหรับการตรวจหาการโป่งพองของหลอดเลือดในสมองนั้น ปัจจุบันแนะนำการตรวจด้วย CT angiography ซึ่งจะสามารถตรวจพบได้ทั้งก้อนเลือดที่คั่งอยู่ในเนื้อสมองซึ่งอาจจะต้องรีบให้การรักษาด้วยการผ่าตัด และการตรวจหาหลอดเลือดจุดที่ผิดปกติ ด้วยเทคนิคดังกล่าวนี้จะสามารถตรวจหาหลอดเลือดที่โป่งพองขนาดตั้งแต่ 2 มิลลิเมตรขึ้นไปได้ อย่างไรก็ตาม ในกรณีที่ภายในจุดที่เกิดการโป่งพองนั้นหากมีลิ่มเลือดก่อตัวอยู่ภายในก็อาจทำให้ตรวจไม่พบก็ได้ เทคนิคอื่น ๆ ที่อาจนำมาใช้ร่วมกับการตรวจ CT angiography ได้แก่ การทำ digital subtraction angiography และเทคนิคการสร้างภาพในแบบ 2 มิติ และ 3 มิติ (2-dimensional and 3-dimensional reconstruction) ซึ่งช่วยเพิ่มความไวในการตรวจวินิจฉัยให้มากขึ้นอย่างมาก และสามารถนำข้อมูลไปใช้ในการวางแผนการรักษาต่อไปได้
การรักษาทางยาเพื่อป้องกันความเสี่ยงในการเกิดเลือดออกซ้ำ
ผู้ป่วยที่เกิดมีเลือดออกซ้ำมีโอกาสในการเสียชีวิตหรือมีความพิการมากกว่าผู้ป่วยที่มีเลือดออกเพียงครั้งเดียวอย่างมาก โดยผู้ป่วยที่มีเลือดออกครั้งแรกจะมีโอกาสเกิดเลือดออกซ้ำภายใน 24 ชั่วโมงแรกราว 4-14% และความเสี่ยงในการเกิดเลือดออกซ้ำจะยังสูงต่อไปได้อีกถึง 30 วันหากยังไม่ได้รับการรักษา การรักษาที่อาจพิจารณาให้ในผู้ป่วยกลุ่มนี้ ได้แก่
1. ยาลดความดันโลหิต เนื่องจากมีข้อมูลพบว่าโรคความดันโลหิตสูงเป็นปัจจัยเสี่ยงที่สำคัญของการเกิดเลือดออกซ้ำ แต่ในปัจจุบันระดับความดันโลหิตเป้าหมายในการรักษาเพื่อป้องกันการมีเลือดออกซ้ำยังไม่เป็นที่กำหนดแน่ชัด เนื่องจากไม่ได้มีข้อมูลจากการศึกษาวิจัยที่ชัดเจน
2. ยาต้านการสลายลิ่มเลือด (antifibrinolytic drugs) อาจช่วยทำให้ลิ่มเลือดที่เกิดขึ้นแล้วคงอยู่ต่อไปได้อีก ซึ่งจะช่วยลดโอกาสในการเกิดเลือดออกซ้ำได้ จากการศึกษาแบบ randomized controlled trial พบว่าผู้ป่วยได้รับยา antifibrinolytics มีเลือดออกซ้ำราวร้อยละ 2 เทียบกับร้อยละ 11 ในกลุ่มที่ไม่ได้รับการรักษา อย่างไรก็ตาม ไม่พบว่าการรักษาด้วยวิธีินี้จะทำให้ผลการรักษาโดยรวมเปลี่ยนแปลงไปจากการไม่ให้ยา ดังนั้น จึงอาจพิจารณาให้ในเฉพาะกลุ่มผู้ป่วยที่ต้องการให้ลิ่มเลือดคงอยู่ได้นานขึ้นในระหว่างที่กำลังรอให้การรักษาจำเพาะ และในระหว่างการรักษาควรเฝ้าระวังภาวะแทรกซ้อนจากการใช้ยา เช่น การมีลิ่มเลือดอุดตันในหลอดเลือดดำที่ขา (deep vein thrombosis) และ delayed cerebral ischemia เป็นต้น
3. การให้ยากันชัก อาการชักนั้นพบได้บ่อยราว 20% ในผู้ป่วย subarachnoid hemorrhage โดยเฉพาะในผู้ป่วยที่มีลิ่มเลือดอยู่ในเนื้อสมอง ซึ่งอาการชักอาจมีผลทำให้การไหลเวียนเลือดผิดปกติและอาจกระตุ้นทำให้มีเลือดออกซ้ำได้มากขึ้น อย่างไรก็ตาม ในแง่ของการใช้ยากันชักในผู้ป่วยกลุ่มนี้ก็ยังไม่ได้มีข้อมูลชัดเจน และยังไม่ได้มีคำแนะนำให้ใช้ยากันชักเพื่อป้องกันอาการชักในผู้ป่วยทุกราย
การรักษาหลอดเลือดโป่งพองในสมองที่แตก
จากข้อมูลการศึกษาที่ผ่านมาพบว่า การรักษาหลอดเลือดที่มีการโป่งพองและแตกเป็นการรักษาที่มีความปลอดภัยและมีประโยชน์มากในแง่ของการป้องกันการเกิดเลือดออกซ้ำ แต่ควรทำโดยแพทย์ที่มีความชำนาญและประสบการณ์ในการรักษา วิธีการในการรักษาที่ใช้ ได้แก่ การผ่าตัด open surgical clipping และการทำหัตถการ endovascular aneurysm obliteration
Open surgical clipping การรักษาด้วยวิธีนี้จำเป็นต้องมีการผ่าตัดเปิดกะโหลกศีรษะ (craniotomy) โดยมีการใช้กล้องจุลทรรศน์เข้ามาช่วยเพื่อเปิดแยกเยื่อหุ้มสมองส่วน subarachnoid space และโยกส่วนของฐานสมองให้สามารถเห็นได้ชัด หลังจากที่พบจุดโป่งพองของหลอดเลือดแล้วจึงใช้คลิปที่ทำจาก titanium หนีบที่บริเวณก้านของจุดที่โป่งเพื่อให้ส่วนปลายที่โป่งพองแฟบลงแต่ยังสามารถให้เลือดไหลเวียนผ่านหลอดเลือดส่วนที่ปกติไปได้
Endovascular aneurysm obliteration เป็นการทำหัตถการผ่านหลอดเลือดโดยใช้สายสวนสอดเข้าทางหลอดเลือด (นิยมผ่านทาง femoral artery ที่บริเวณขาหนีบ) ไปยังสมองและนำทางด้วย fluoroscope ไปหยุดอยู่เส้นเลือดก่อนถึงจุดโป่งพอง (parent artery) จากนั้นจึงใช้สายสวนขนาดเล็ก (microcatheter) ผ่านเข้าไปในจุดที่โป่งพอง แล้วสอดขดลวดโลหะ (metal coils) เข้าไปภายใน ขดลวดโลหะจะทำให้เลือดที่ไหลเวียนผ่านเข้าไปในจุดที่โป่งพองหยุดลง และกระตุ้นให้เกิดการสร้างลิ่มเลือดขึ้นภายในทำให้จุดโป่งพองนี้อุดตัน และไม่เกิดเลือดออกซ้ำได้
การศึกษาเปรียบเทียบการรักษาแต่ละวิธีข้างต้น ได้แก่ การศึกษา International Subarachnoid Aneurysm Trial (ISAT) และ Barrow Ruptured Aneurysm Trial (BRAT) พบว่าการรักษาด้วยวิธีผ่าตัดมีโอกาสสำเร็จในการอุดหลอดเลือดส่วนที่โป่งพองได้ดีกว่าและคงทนอยู่ได้นานกว่าการรักษาผ่านหลอดเลือด แต่ในแง่ของ functional outcomes 1 ปีหลังการรักษา พบว่าการทำหัตถการผ่านหลอดเลือดให้ผลที่ดีกว่าการผ่าตัด ในทางปฏิบัติแล้ว การรักษาด้วยวิธีการผ่าตัดอาจเป็นทางเลือกที่ดีกว่าหากทำในผู้ป่วยดังต่อไปนี้คือ
1. ผู้ป่วยที่มีความผิดปกติทางระบบประสาทเกิดขึ้นแล้ว
2. มีภาวะความดันภายในกะโหลกศีรษะ (increased intracranial pressure) เพิ่มขึ้น
3. มีหลอดเลือดโป่งพองในตำแหน่งที่มองเห็นได้ยากด้วยการตรวจ angiography
4. จำเป็นต้องได้รับการผ่าตัด revascularization และ bypass ร่วมด้วย
5. เป็นผู้ป่วยที่มีอายุน้อยกว่า 40 ปี ที่มีหลอดเลือดโป่งพองเกิดขึ้นในบริเวณ anterior circulation ซึ่งเป็นกลุ่มผู้ป่วยที่ต้องการป้องกันการเกิดเลือดออกซ้ำต่อไปได้นาน
การรักษาภาวะแทรกซ้อนที่เกิดขึ้นจากภาวะเลือดออกในเยื่อหุ้มสมอง
ภาวะหลอดเลือดสมองหดเกร็งและสมองขาดเลือด ภาวะหลอดเลือดสมองหดเกร็ง (vasospasm) สามารถพบได้ราวร้อยละ 70 ในผู้ป่วยที่เกิดภาวะเลือดออกในเยื่อหุ้มสมอง โดยมักจะเริ่มพบมีความผิดปกติเกิดขึ้นราววันที่ 3-4 หลังเกิดเลือดออก และสูงสุดในวันที่ 7-10 จากนั้นจึงค่อย ๆ ลดลงจนหายไปใน 14-21 วัน ส่วนภาวะสมองขาดเลือดในระยะหลัง (delayed cerebral ischemia) เป็นความผิดปกติของระบบประสาทเฉพาะที่ที่พบได้ราว 1 ใน 3 ของผู้ป่วยทั้งหมด โดยมักจะเกิดขึ้นในช่วง 4-14 วันหลังจากมีเลือดออก และเป็นสาเหตุของการเสียชีวิตและความพิการที่สำคัญมากในผู้ป่วยกลุ่มนี้
ข้อมูลหลักฐานที่ผ่านมาพบว่า การเกิด vasospasm และ delayed cerebral ischemia นี้เป็นผลจากการเปลี่ยนแปลงของระบบไหลเวียนเลือดและระบบประสาทหลายอย่าง แต่การเกิด vasospasm อาจไม่ได้เป็นสาเหตุของ cerebral ischemia เสมอไป เนื่องจากมีข้อมูลการศึกษาที่พบว่า nimodipine ซึ่งสามารถช่วยลดความเสี่ยงของการเกิดภาวะ delayed cerebral ischemia นั้นไม่ได้ออกฤทธิ์ขยายหลอดเลือดในส่วนที่เกิด vasospasm และการรักษาที่ทำให้ภาวะ vasospasm ลดลงนั้นกลับไม่ได้ช่วยทำให้โอกาสในการเกิด cerebral ischemia ลดลง ดังนั้น อาจมีปัจจัยอื่นที่มีความเกี่ยวข้องเชื่อมโยงกัน และยังจำเป็นต้องมีการศึกษาเพิ่มเติมต่อไป
ในปัจจุบันในแง่ของการป้องกันภาวะ delayed cerebral ischemia นั้น หลักฐานจาก Cochrane review แนะนำการใช้ nimodipine ชนิดรับประทานตั้งแต่แรกวินิจฉัยไปจนถึง 21 วัน เนื่องจากสามารถลดโอกาสเกิดภาวะแทรกซ้อนลงได้ราว 1 ใน 3 นอกจากนี้ควรดูแลให้ระบบไหลเวียนเลือดและมีระดับ hemoglobin มากเพียงพอ แต่ไม่ควรมากเกินและไม่ควรทำ balloon angioplasty เพื่อรักษาภาวะ vasospasm
สำหรับผู้ป่วยที่มีระดับความรู้สึกตัวลดลงอยู่ก่อน การตรวจร่างกายเพื่อค้นหาภาวะ delayed cerebral ischemia อาจทำได้ยาก กรณีนี้อาจพิจารณาทำการตรวจด้วยวิธี transcranial Doppler ultrasonography ซึ่งจะสามารถตรวจพบ vasospasm หรือการตรวจ perfusion CT scan เพื่อค้นหาตำแหน่งของการเกิด ischemia แทนได้ และหากพบมีความผิดปกติควรให้การรักษาโดยให้สารน้ำทางหลอดเลือดให้มากขึ้น ร่วมกับการใช้ยาในกลุ่ม alpha-adrenergic agents เพื่อเพิ่มการไหลเวียนเลือดไปยังสมอง
ภาวะน้ำคั่งในช่องสมอง (hydrocephalus) พบได้ประมาณ 15-85% แต่ส่วนใหญ่แล้วมักจะไม่รุนแรงและไม่มีความสำคัญทางคลินิกชัดเจน อาการอาจเกิดได้อย่างรวดเร็วหรือช้ากินเวลาหลายวันหรือหลายสัปดาห์ได้ จึงต้องสงสัยไว้เสมอในรายที่มีอาการแย่ลงหลังจากที่ดีขึ้นแล้วในระยะแรก ในรายที่เกิดมีอาการรุนแรง เช่น ทำให้ระดับความรู้สึกตัวเปลี่ยนแปลงควรให้การรักษาโดยใส่ external ventricular drain ซึ่งสามารถทำให้อาการทางระบบประสาทดีขึ้นได้ ในบางรายที่มีอาการต่อเนื่องนานหรือเรื้อรัง (พบได้ราว 1 ใน 3 ของผู้ป่วยที่เกิด acute hydrocephalus) อาจพิจารณาเลือกใส่ ventriculoperitoneal shunt ได้
สรุป
ภาวะเลือดออกในเยื่อหุ้มสมองเป็นภาวะที่มีความสำคัญเนื่องจากสามารถทำให้เสียชีวิตหรือมีความพิการได้ สาเหตุส่วนใหญ่มักเกิดขึ้นจากการโป่งพองของหลอดเลือดในสมองและมีเลือดออกจากจุดที่โป่งพอง หลังจากที่เกิดเลือดออกแล้ว ความเสี่ยงในการเกิดเลือดออกซ้ำจะยังคงสูงอยู่ได้ถึง 30 วันแรก ดังนั้น ผู้ป่วยจึงควรได้รับการตรวจและรักษาการโป่งพองของหลอดเลือดดังกล่าวเพื่อป้องกันการกลับเป็นซ้ำ วิธีการในการรักษาอาจทำได้ทั้งการผ่าตัด และการทำหัตถการด้วยสายสวนผ่านหลอดเลือด ทั้งนี้การผ่าตัดอาจเป็นทางเลือกที่เหมาะสมกว่าในผู้ป่วยเฉพาะราย
References
- Rincon F, Rossenwasser RH, Dumont A. The epidemiology of admissions of nontraumatic subarachnoid hemorrhage in the United States. Neurosurgery 2013;73:217-22.
- Johnston SC, Selvin S, Gress DR. The burden, trends, and demographics of mortality from subarachnoid hemorrhage. Neurology 1998;50:1413-8.
- Taufique Z, May T, Meyers E, et al. Predictors of poor quality of life 1 year after subarachnoid hemorrhage. Neurosurgery 2016;78:256-64.
- Elhadi AM, Zabramski JM, Almefty KK, et al. Spontaneous subarachnoid hemorrhage of unknown origin: hospital course and long-term clinical and angiographic follow-up. J Neurosurg 2015;122: 663-70.
- Brown RD Jr, Broderick JP. Unruptured intracranial aneurysms: epidemiology, natural history, management options, and familial screening. Lancet Neurol 2014;13:393-404.
- Kataoka K, Taneda M, Asai T, Kinoshita A, Ito M, Kuroda R. Structural fragility and inflammatory response of ruptured cerebral aneurysms: a comparative study between ruptured and unruptured cerebral aneurysms. Stroke 1999;30:1396-401.
- Bor AS, Koffijberg H, Wermer MJ, Rinkel GJ. Optimal screening strategy for familial intracranial aneurysms: a cost-effectiveness analysis. Neurology 2010;74:1671-9.
- Broderick JP, Brown RD Jr, Sauerbeck L, et al. Greater rupture risk for familial as compared to sporadic unruptured intracranial aneurysms. Stroke 2009;40:1952-7.
- Lall RR, Eddleman CS, Bendok BR, Batjer HH. Unruptured intracranial aneurysms and the assessment of rupture risk based on anatomical and morphological factors: sifting through the sands of data. Neurosurg Focus 2009;26(5):E2.
- Wiebers DO, Whisnant JP, Huston J III, et al. Unruptured intracranial aneurysms: natural history, clinical outcome, and risks of surgical and endovascular treatment. Lancet 2003;362:103-10.
- Ingall T, Asplund K, Mähönen M, Bonita R. A multinational comparison of subarachnoid hemorrhage epidemiology in the WHO MONICA stroke study. Stroke 2000;31:1054-61.
- de Rooij NK, Linn FH, van der Plas JA, Algra A, Rinkel GJ. Incidence of subarachnoid haemorrhage: a systematic review with emphasis on region, age, gender and time trends. J Neurol Neurosurg Psychiatry 2007;78:1365-72.
- Korja M, Lehto H, Juvela S, Kaprio J. Incidence of subarachnoid hemorrhage is decreasing together with decreasing smoking rates. Neurology 2016;87:1118-23.
- Shea AM, Reed SD, Curtis LH, Alexander MJ, Villani JJ, Schulman KA. Characteristics of nontraumatic subarachnoid hemorrhage in the United States in 2003. Neurosurgery 2007;61:1131-8.
- Nieuwkamp DJ, Setz LE, Algra A, Linn FH, de Rooij NK, Rinkel GJ. Changes in case fatality of aneurysmal subarachnoid hemorrhage over time, according to age, sex, and region: a meta-analysis. Lancet Neurol 2009;8:635-42.
- Huang J, van Gelder JM. The probability of sudden death from rupture of intracranial aneurysms: a meta-analysis. Neurosurgery 2002;51:1101-7.
- Bassi P, Bandera R, Loiero M, Tognoni G, Mangoni A. Warning signs in subarachnoid hemorrhage: a cooperative study. Acta Neurol Scand 1991;84:277-81.
- Polmear A. Sentinel headaches in aneurysmal subarachnoid hemorrhage: what is the true incidence? A systematic review. Cephalalgia 2003;23:935-41.